Vacuna Sars - Cov - 2 y Leche materna
Marzo - 2021
Vacuna de ARNm BNT162b2 COVID-19 provoca una respuesta de anticuerpos rápida y sincronizada en sangre y leche materna.
Michal Rosenberg https://www.medrxiv.org/content/10.1101/2021.03.06.21252603v1
Se describe dinámica de respuesta de anticuerpos específicos de vacuna en leche materna y suero en una cohorte prospectiva de diez mujeres amamantando que recibieron dos dosis de vacuna de ARNm de Pfizer-BioNTech BNT162b2 COVID-19. La respuesta de anticuerpos fue rápida y altamente sincronizada entre la leche materna y el suero, alcanzando la estabilización 14 días después de la segunda dosis. El anticuerpo sérico predominante fue IgG. La respuesta en leche materna incluyó tanto IgG como IgA con capacidad neutralizante.
La campaña acelerada de vacunación COVID-19 en Israel se inició en
diciembre de 2020 y actualmente casi el 50% de la población adulta
ha recibido la vacuna Pfizer-BioNTech BNT162b2 COVID-19 mRNA (vacuna
mRNA) 1. La campaña de vacunación se dirigió inicialmente
a poblaciones de alto riesgo (≥
60 años y proveedores de
atención médica) 2 y pronto se expandió a mujeres que
amamantan3. A pesar de la alta eficacia informada
de esta vacuna4 y la evidencia de generación de
anticuerpos virales específicos en la leche materna de mujeres con
COVID-195-7, no hay datos disponibles sobre su eficacia
en mujeres que amamantan o sus posibles beneficios en la protección
neonatal a través de la transferencia pasiva de anticuerpos
específicos - vacuna en la leche materna 8.
La brecha de conocimiento
actual impide que las autoridades sanitarias mundiales formulen
recomendaciones concretas sobre la vacunación durante la lactancia.
Se describe la dinámica de la respuesta de anticuerpos séricos y de leche materna en una cohorte prospectiva de diez proveedores de atención de salud ammantando, con una edad promedio de 34.6 años (rango 30-38), que recibieron la primera dosis de vacuna de ARNm aproximadamente cinco meses después del parto (promedio de 154 días, rango 68-382) y la segunda dosis 21 días después (Tabla complementaria 1).
Para obtener los títulos finales de IgG e IgA en diadas leche materna y suero contra las proteínas spike (espiga) y dominio de unión al receptor (RBD) del SARS-CoV-2, se realizaron pruebas ELISA seriadas los días 7 y 14 después de la primera (designados 1D7 y 1D14, respectivamente) y segunda dosis de vacuna (designadas 2D7 y 2D14, respectivamente) (Fig. 1 complementaria y Fig. 2 complementaria).
Se encontró que las respuestas de anticuerpos específicos anti- spike (Figura 1) y anti - RBD (Figura 3 complementaria) en leche materna y el suero eran sincronizadas para IgG e IgA.
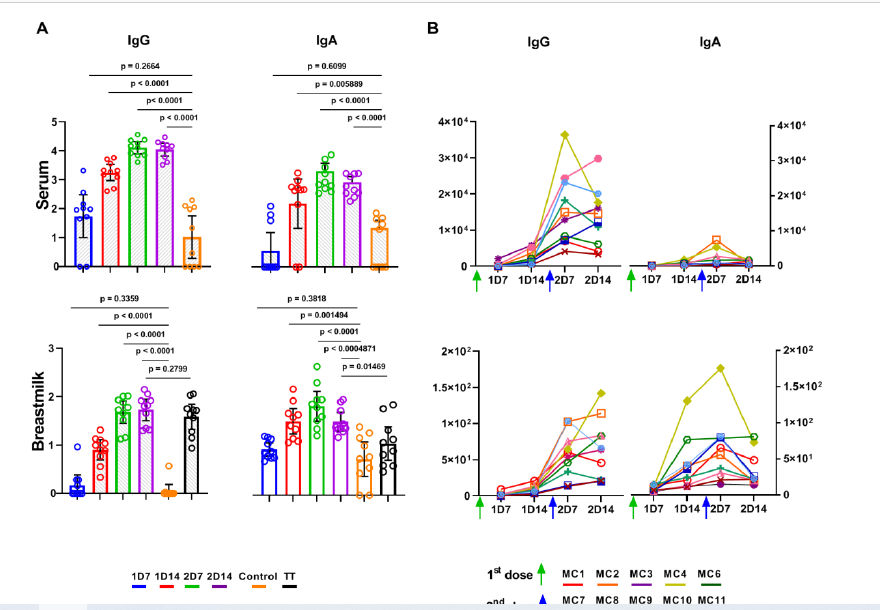
Figura 1.- Títulos de anticuerpos IgG e IgA específicos anti - spike en leche materna y suero de madres vacunadas con vacuna Pfizer-BioNTech (n = 10).
A.- Títulos finales se interpolaron aplicando una curva logística de 4 parámetros en diluciones seriadas recíprocas para IgG e IgA para todas las muestras de suero y lactosuero en 4 momentos (por color) y para IgG e IgA específicas del toxoide tetánico (TT) en leche materna. P < 0.0083 = estadísticamente significativo. Los resultados se presentan como medias geométricas e intervalos de confianza del 95%. Unidades eje Y son títulos anticuerpos en escala logarítmica. Se obtuvieron muestras de suero control (n = 10) y lactosuero (n = 10) antes de la pandemia de COVID-19.
(B) Títulos anticuerpos por participante, cada uno mostrado en un color diferente. Las flechas verdes y azules indican momento de administración de primera (t = 0) y segunda (t = 21) dosis de vacuna, respectivamente. Las unidades del eje Y son títulos de anticuerpos en escala lineal.
En 1D7, los títulos de
anticuerpos vacuna específicos no habían aumentado
significativamente por encima de los títulos en grupo control (suero
prepandémico y lactosuero) y el primer aumento significativo en los
títulos de anticuerpos fue evidente en 1D14. La tendencia ascendente
alcanzó su punto máximo en 2D7, seguida de ligera disminución en
títulos en 2D14.
Dado que todos las
participantes habían recibido la vacuna contra tétanos, difteria y
tos ferina acelular (DTPa) durante el tercer trimestre9,
se pudo comparar los títulos de anticuerpos IgG e IGA en leche
materna para IgG e IgA provocados por vacuna de ARNm en 2D14 con
título de anticuerpo específico - toxoide tetánico (TT) en las
mismos participantes. Encontramos que títulos de IgG e IgA
específicos spike y RBD no diferían significativamente de títulos de
anticuerpos específicos de TT.
Posteriormente, evaluamos la relación IgG / IgA específica de vacuna en leche materna y suero. La respuesta de anticuerpos en suero estuvo dominada por IgG, y la relación IgG / IgA fue significativamente mayor en suero que en leche materna en los 4 puntos de tiempo (Figura 4 complementaria). La relación IgG / IgA en la leche materna indicó que la respuesta vacuna - específica no estuvo dominada por IgA, sino más bien que la relación IgG / IgA aumentó con el tiempo, como se describió previamente después de la inmunización para virus respiratorio sincitial10.
Para comprender mejor la
dinámica en el tiempo de la respuesta de anticuerpos después de la
vacunación con ARNm, calculamos el cambio de veces de los títulos
finales en cada punto de tiempo en comparación con el punto de
tiempo anterior. Los títulos de IgG e IgA vacuna - específicos
en leche materna y suero aumentaron sustancialmente 7 días después
de cada dosis de vacuna, y el aumento en cambio de veces se detuvo
14 días después de la segunda dosis.
Es de destacar que para IgA
específica para Spike y RBD en leche materna, el cambio de veces en
2D14 cayó por debajo de 1, lo que indica disminución de los niveles
de IgA en ese momento (Figura
5 complementaria). El
cálculo del cambio de veces por encima del título de punto final en
1D7 (Figura 2, Figura complementaria 6) mostró que la dinámica de la
respuesta vacuna - específica en suero y leche materna se estabilizó
en 2D14, ya que el cambio de veces en 2D14 no fue significativamente
más alto que en el punto de tiempo anterior.
Finalmente, evaluamos la fracción de anticuerpos neutralizantes en leche materna con un estudio de bloqueo competitivo in vitro desarrollado previamente11. Tanto la IgG como la IgA anti-spike en leche materna de todas las participantes exhibieron una capacidad de neutralización potencial [en promedio, 13% de los anticuerpos vacuna - específicos se bloquearon en el estudio (Figura 7 complementaria). Es de destacar que una publicación reciente6 reportó que se encontró que solo 62% de las muestras de leche materna (que contienen anticuerpos) de mujeres con COVID-19 tenían capacidad neutralizante in vitro.
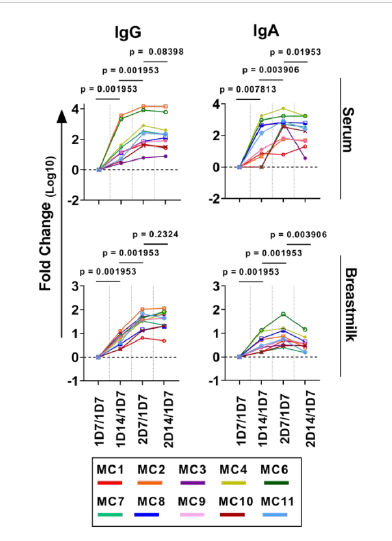
Figura 2.- Dinámica de
respuesta de anticuerpos vacuna - específicos IgG e IgA y capacidad
de neutralización de anticuerpos. Los cambios de veces en títulos
anticuerpos en comparación con la primera dosis vacuna en primer
momento se grafican por paciente. P < 0.05 = estadísticamente
significativo. Las unidades del eje Y son cambios de veces en escala
logarítmica.
La importancia de la lactancia
materna en la primera infancia se destaca por la fuerte correlación
entre lactancia materna y abrumadora disminución de los riesgos de
infección y la morbilidad y mortalidad asociadas a infección12,13.
La lactancia materna se ha asociado con una disminución en el número
de casos de enfermedades respiratorias14,
disminución del riesgo de hospitalización por enfermedades
respiratorias15,16 y protección contra una amplia gama de
infecciones que pueden colonizar el intestino17,18. Los
casos reportados de pacientes con COVID-19 que experimentaron
síntomas relacionados con el tubo digestivo19 y la
detección de ARN viral en muestras de heces20 sugieren
una posible vía de transmisión fecal-oral21.
En resumen, el estudio proporciona evidencia de la rápida producción
de anticuerpos específicos de la vacuna, tanto IgA como IgG. Además,
se observó capacidad neutralizante en todas las muestras. Este
estudio también indica la protección potencial de los bebés
amamantados mediante la administración de la vacuna BNT162b2 COVID-19
a la madre que amamanta.